Traitement par ventilation mécanique à domicile
Les patients ventilés ont des besoins complexes et évolutifs qui nécessitent une prise en charge et une surveillance attentives. Découvrez comment les technologies de ventilation avancées sont conçues pour favoriser une titration, une surveillance et une ventilation efficaces, et découvrez les solutions ResMed qui pourraient améliorer l’expérience de vos patients.
FAQ: le processus de titration
L’objectif premier de la ventilation mécanique est d’améliorer les échanges gazeux pulmonaires et de faciliter la récupération des muscles respiratoires fatigués en leur donnant un repos suffisant.6 Après une évaluation de base, la ventilation mécanique est mise en place avec des réglages standard. Les paramètres du ventilateur, tels que le volume courant, la fréquence respiratoire, la PEP et la FiO2, sont ensuite ajustés. Le confort du patient et la synchronisation patient-ventilateur sont pris en compte, et les réglages sont réévalués pour s’assurer que le traitement est adapté aux besoins et aux préférences du patient.
Voici quelques exemples de questions que vous pourriez vous poser pendant la titration.
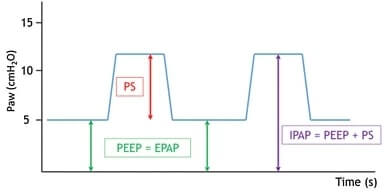
PS (Pressure Support) est la différence de pression entre l’IPAP (Inspiratory Positive Airway Pressure, ou PIP pression inspiratoire positive en français) et l’EPAP (Expiratory Positive Airway Pressure, ou PEP pression expiratoire positive) qui est délivrée par le ventilateur à chaque respiration. La PS définit la quantité d’air que le patient reçoit à chaque respiration et permet de corriger l’hypoventilation alvéolaire nocturne. Certains ventilateurs utilisent des paramètres tels que « IPAP/EPAP » ou « PS/PEEP » pour régler automatiquement la PS ou l’IPAP. 7
Les réglages de la PEP ont des objectifs différents en fonction de la pathologie traitée. Chez les patients souffrant de pathologies obstructives telles que la BPCO, la PEP intrinsèque est fréquente. Ces patients peuvent avoir du mal à terminer leur expiration, mais la PEP les aide en réduisant l’effort respiratoire nécessaire pour déclencher une respiration. Dans des pathologies telles que le syndrome d’obésité-hypoventilation (SOH), un réglage approprié de la PEP peut prévenir l’affaissement des voies aériennes supérieures pendant le sommeil7.
Il est essentiel d’ajuster progressivement l’EPAP tout en observant l’effort du patient. Si la PEP est réglée trop bas, le patient peut avoir du mal à déclencher l’inspiration efficacement, ce qui peut entraîner un retard de déclenchement, des efforts inefficaces, l’épuisement et la non-observance. Inversement, si la PEP est réglée à un niveau trop élevé, elle peut entraîner des fuites et un inconfort pour le patient. 7
L’algorithme AutoEPAP de ResMed ajuste automatiquement la PEP pour maintenir les voies aériennes supérieures ouvertes.
Il est disponible sur les appareils Lumis ST, ST-A, Stellar 150 et Astral. Vous souhaitez en savoir plus ? Découvrez l’AutoEPAP de ResMed.
Une fréquence de secours déclenche le ventilateur pour fournir une assistance lorsque le patient ne respire pas suffisamment par lui-même. En configurant une fréquence de secours, vous pouvez vous assurer que votre patient recevra une ventilation adéquate à tout moment. La fréquence de secours est généralement réglée à un niveau légèrement inférieur à la fréquence spontanée du patient, ce qui favorise les respirations déclenchées par le patient.7 L’absence de fréquence de secours est associée à un nombre accru d’événements mixtes et centraux des voies aériennes supérieures chez les patients souffrant du syndrome obésité-hypoventilation8.
Le temps de montée est le temps nécessaire au ventilateur pour passer de la PEP à la PIP. Le temps de montée peut être ajusté en fonction des besoins ventilatoires du patient, de son type de maladie et de sa condition physique. Cela peut contribuer à améliorer le travail respiratoire, le confort et la synchronisation. Les patients ayant une forte demande ventilatoire, comme ceux atteints de BPCO, peuvent se sentir plus à l’aise avec un temps de montée plus rapide ; d’autres, comme ceux atteints de MNM, peuvent préférer un rythme plus lent. 7
Tous les ventilateurs ResMed sont dotés de la fonction temps de montée, qui vous permet de régler avec précision le temps nécessaire à l’appareil pour atteindre la PIP. Envie d’en savoir plus ? Découvrez les fonctions temps de montée et temps de descente de ResMed.
Le temps de descente est le temps nécessaire pour que la pression des voies aériennes passe de la PIP à la PEP lorsque le cycle se produit. Le temps de transition vers l’expiration varie d’une personne à l’autre. Le réglage du temps de descente en fonction des besoins physiques et des préférences du patient peut améliorer la synchronisation patient-appareil et le confort respiratoire, en particulier pour les personnes dont le débit expiratoire est limité. Il est généralement admis qu’un temps de descente réglable peut être particulièrement utile pour les patients souffrant d’une BPCO avancée, bien qu’il faille noter que la recherche clinique dans ce domaine est actuellement insuffisante. Ces patients peuvent ressentir un petit affaissement des voies respiratoires lors de l’expiration, ce qui pourrait être atténué par un temps de descente plus long.7
La fonction temps de descente de ResMed vous permet de personnaliser le temps nécessaire à l’appareil de votre patient pour atteindre la PEP. Elle est disponible sur les appareils Stellar. Envie d’en savoir plus ? Découvrez les fonctions temps de montée et temps de descente de ResMed.
Le déclenchement, ou déclenchement inspiratoire, détermine le moment où l’inspiration du patient commence. La sensibilité du déclenchement est un paramètre crucial pour assurer la synchronisation patient-ventilateur. Un déclenchement moyen peut convenir lorsque le patient est éveillé, mais le niveau de sensibilité doit être adapté à la période de sommeil afin d’éviter les efforts inspiratoires inefficaces. 7
La fonction Déclenchement et cyclage de ResMed vous permet de régler avec précision l’effort requis pour démarrer et terminer un cycle respiratoire. Elle est disponible sur tous les ventilateurs ResMed. Envie d’en savoir plus ? Découvrez les réglages de déclenchement et de cyclage ResMed.
Le cycle, ou déclencheur expiratoire, détermine le moment où l’inspiration se termine. La sensibilité au cycle est donc un paramètre crucial qui sous-tend la synchronisation patient-ventilateur. Idéalement, le cycle du ventilateur doit s’aligner sur le cycle respiratoire naturel du patient. Un cycle prématuré (l’administration d’air s’arrête trop rapidement), et un cycle tardif (le ventilateur continue d’administrer de l’air après la fin de la respiration du patient) peuvent tous deux nuire au confort du patient. Le déclencheur expiratoire doit être ajusté pour obtenir un temps d’inspiration qui reflète la mécanique respiratoire du patient et son état obstructif ou restrictif.7
Tous les ventilateurs ResMed sont dotés de la fonction déclenchement et cyclage qui vous permet de régler avec précision l’effort requis pour démarrer et terminer un cycle respiratoire. Envie d’en savoir plus ? Découvrez les réglages de déclenchement et de cyclage ResMed.
Lorsqu’un patient déclenche une respiration et que le ventilateur est en mode d’assistance en pression (PS), le temps d’inspiration est déterminé par l’effort du patient et la mécanique respiratoire, ainsi que par des paramètres spécifiques du ventilateur tels que le temps de montée en pression, la PIP et la sensibilité de déclenchement de l’expiration. En définissant un temps d’inspiration maximal (TiMax), vous pouvez limiter la durée de la phase d’inspiration. Cela peut être utile dans les situations où des fuites d’air importantes, des retards dans l’atteinte du critère de cyclage du débit ou des difficultés à faire correspondre le rythme d’inspiration naturel du patient peuvent amener le ventilateur à passer trop de temps dans la phase inspiratoire. Un temps d’inspiration minimum (TiMin) peut également être défini pour garantir un temps d’inspiration suffisant, en vue d’améliorer la ventilation alvéolaire.7
La fonction TiControl de ResMed définit des limites minimales et maximales pour le temps d’inspiration afin de répondre aux besoins d’inspiration naturels du patient. Elle est disponible sur tous les ventilateurs ResMed. Envie d’en savoir plus ? Découvrez ResMed TiControl.
Pour s’assurer que le patient reçoit bien la pression prescrite au niveau du masque, le circuit respiratoire et l’interface patient doivent être configurés et calibrés afin que le ventilateur puisse mesurer et compenser la résistance du circuit. La configuration du type de masque dans l’algorithme du ventilateur facilite également le contrôle des fuites intentionnelles et l’estimation des fuites non intentionnelles.7
Mise en place des soins à distance

La VNI à domicile est souvent mise en place dans les hôpitaux. Ce processus est coûteux et mobilise beaucoup de ressources pour les professionnels de santé. Il n’est pas pratique pour les patients, en particulier ceux qui souffrent de maladies graves ou de handicaps sévères, qui doivent se déplacer et passer du temps loin de chez eux dans un environnement hospitalier stressant. Heureusement, des essais ont montré que la mise en place de la VNI à domicile pour les patients atteints de maladies neuromusculaires, de maladies thoraciques restrictives et de BPCO est aussi efficace que la mise en place en milieu hospitalier et réduit les coûts de plus de 50%5.
FAQ: Suivi à distance
Le télésuivi peut être utilisé pour gérer les patients ventilés de différentes manières. L’accès aux données pertinentes vous permet de surveiller et de suivre l’évolution de l’état clinique et des paramètres de l’appareil d’un individu ou d’un groupe de patients. De plus, les notifications peuvent vous alerter lorsqu’un patient nécessite une attention particulière. La possibilité de contrôler et d’ajuster à distance les paramètres de l’appareil de votre patient facilite encore davantage l’efficacité et la rapidité des soins, et vous aide à favoriser l’adhésion et l’efficacité du traitement à un stade précoce. Grâce au télésuivi, les patients ont une meilleure qualité de vie, moins de réadmissions à l’hôpital et un risque réduit d’exacerbations 9-11.
Les ventilateurs peuvent enregistrer toute une série de données, notamment l’utilisation, l’IAH, la pression des voies aériennes, le débit, le volume courant, les fuites, les temps d’inspiration et d’expiration, le déclenchement et le cycle, ainsi que la fréquence respiratoire. Les ventilateurs peuvent enregistrer ces variables avec une grande précision et stocker les données sur une carte mémoire, une clé USB ou dans le cloud. Certains ventilateurs peuvent télécharger automatiquement les données vers des plateformes de gestion des patients pour une surveillance à distance.
Le système de gestion des patients AirView de ResMed vous permet d’accéder, d’analyser et de partager facilement les données respiratoires de vos patients et de suivre l’évolution de leur état clinique. Envie d’en savoir plus ?
Si un patient commence à moins utiliser son ventilateur, cela peut indiquer qu’il a du mal à tolérer son traitement, par exemple en raison d’effets indésirables ou de réglages inadéquats. De même, une utilisation accrue du ventilateur peut indiquer un besoin accru d’assistance respiratoire, peut-être en raison de la progression de la maladie. L’utilisation quotidienne totale de la VNI par le patient est enregistrée sous forme de statistiques et de tendances.10
Les fuites involontaires constituent un événement indésirable fréquent dans le cadre de la VNI. Elles affectent la qualité de la ventilation et peuvent entraîner une diminution de l’observance, un asynchronisme patient-ventilateur et une détérioration de la qualité du sommeil. Les données détaillées de télésurveillance peuvent aider les cliniciens et les prestataires de soins à domicile à identifier et à gérer les fuites involontaires à distance. Les statistiques et les tendances relatives aux fuites peuvent être utilisées pour déterminer où et pourquoi une fuite se produit et permettre la résolution des fuites, ce qui est associé à une amélioration de l’efficacité de la VNI. 10 L’utilisation des données du ventilateur facilite la détection précoce et objective des fuites et l’adaptation ultérieure des paramètres.10
Les données du ventilateur peuvent être utilisées pour examiner le score IAH (indice d’apnée-hypopnée) du patient et sa courbe de débit. L’IAH mesure le nombre de fois où la respiration du patient s’arrête ou est considérablement réduite pendant chaque heure de sommeil. L’IAH est une mesure utile pour les patients souffrant d’apnée obstructive du sommeil ou du syndrome d’obésité-hypoventilation s’il n’y a pas de fuites involontaires. Il peut manquer des obstructions des voies aériennes supérieures si des fuites ou des blocages laryngés sont présents. L’examen de la forme d’onde du débit peut aider les cliniciens à identifier les événements que l’IAH ne détecte pas. La forme de l’onde peut suggérer la cause des obstructions des voies aériennes supérieures, bien qu’une polygraphie puisse être nécessaire pour la confirmer.
La synchronisation patient-ventilateur est évaluée à l’aide de statistiques et peut être examinée de près dans les formes d’ondes de pression et de débit. La synchronisation globale est affichée avec le pourcentage de respirations déclenchées et cycliques spontanément. Ces valeurs dépendent de divers facteurs et doivent être interprétées avec prudence. Par exemple, le pourcentage de respirations déclenchées peut être surestimé en cas de déclenchement automatique et ne pas tenir compte des efforts inefficaces ou des fuites involontaires. Le pourcentage de respirations cycliques spontanées est influencé par les réglages des critères de cyclage, la plage de temps d’inspiration et les fuites involontaires. Une analyse détaillée implique l’interprétation des formes d’ondes de pression et de débit sur un axe temporel spécifique, par exemple 1 minute par période. Cela permet d’identifier les asynchronies de phase (efforts inefficaces, auto-déclenchement, cyclage prématuré, double déclenchement et cyclage retardé) et les asynchronies de débit (dépassement de débit ou débit insuffisant).10
L’oxymétrie de pouls nocturne est un outil de dépistage simple et rentable pour évaluer l’impact de la VNI sur les échanges gazeux. L’oxymétrie de pouls nocturne, qu’elle soit autonome ou connectée à un ventilateur, permet un examen visuel de la SpO2, des fuites et des formes d’ondes. Elle permet de détecter une désaturation rapide en cas d’obstruction des voies aériennes supérieures. Bien qu’il ne soit pas recommandé pour certaines populations, il permet de dépister les événements respiratoires, de prédire les résultats et de surveiller l’utilisation de la VNI pendant la nuit. L’interprétation de l’oxymétrie de pouls nocturne nécessite au moins 4,5 heures d’enregistrement du sommeil avec un minimum d’artefacts, à l’exclusion des fuites involontaires. L’inspection visuelle complète les statistiques en raison de leurs limites. Des résultats anormaux peuvent entraîner des ajustements du ventilateur.10
FAQ ventilation mécanique
La ventilation non invasive (VNI) désigne tout type de ventilation délivrée par une interface non invasive telle qu’un masque nasal, un masque facial ou un embout buccal. Elle est couramment utilisée pour traiter l’insuffisance respiratoire, qui survient lorsque le système respiratoire ne parvient pas à échanger correctement les gaz (oxygène et dioxyde de carbone) dans le corps. Au fur et à mesure que la technologie s’améliore, la ventilation non invasive devient un moyen de plus en plus populaire d’assurer la ventilation mécanique. La ventilation non invasive est conçue pour fournir une ventilation efficace sans qu’il soit nécessaire de procéder à une intubation ou à une trachéotomie. La VNI est donc plus facile à mettre en œuvre et plus confortable pour le patient. Elle réduit également le risque d’infection par rapport aux méthodes invasives.12 La VNI est conçue pour offrir plus de flexibilité aux patients non dépendants, car la ventilation peut être intermittente. Par exemple, ils peuvent recevoir un traitement uniquement pendant la nuit, rester en dehors des unités de soins intensifs et être plus facilement traités à leur domicile.
La ventilation invasive (IV) est généralement utilisée chez les patients pour lesquels la ventilation non invasive (VNI) échoue. Le terme « invasive » est utilisé si le traitement implique un instrument pénétrant par la bouche (par exemple une sonde endotrachéale), le nez ou la peau (par exemple une sonde de trachéotomie) pour servir de voie respiratoire artificielle. Elle est parfois utilisée lorsqu’un patient souffre d’insuffisance respiratoire aiguë ou dépend d’une ventilation à domicile de longue durée. Avec un tuyau de trachéotomie en place, les fuites peuvent être contrôlées et la ventilation assurée. Pour les patients ayant des sécrétions excessives, la trachéotomie permet un accès direct pour l’élimination des sécrétions par aspiration.
La ventilation mécanique, qu’elle soit invasive ou non invasive, envoie de l’air pour gonfler les poumons, un peu comme une personne souffle pour gonfler un ballon. Pour ce faire, elle envoie de l’air à une pression prédéfinie (ventilation barométrique) ou à un volume prédéfini (ventilation volumétrique) pendant la phase d’inspiration du cycle respiratoire du patient.
La ventilation barométrique délivre une pression prédéfinie à chaque inspiration, mais le volume courant et le débit du patient ne sont pas fixes et peuvent varier à chaque respiration. Les ventilateurs bi-level fournissent généralement une ventilation barométrique et utilisent un circuit de fuite. Ils sont principalement utilisés pour la ventilation non invasive (VNI), bien que certains puissent être utilisés pour des patients non dépendants, ventilés de manière invasive.
La ventilation volumétrique délivre un volume d’air prédéfini pendant la période inspiratoire. La pression nécessaire pour délivrer ce volume varie et le débit peut être ajusté.
Les modes hybrides combinent les aspects de la ventilation volumétrique et de la ventilation barométrique. Cela garantit que le volume de pression dans les voies respiratoires qui est délivré est continuellement ajusté pour atteindre le volume prédéfini.
En règle générale, la ventilation invasive (IV) est assurée par un ventilateur capable de délivrer des pressions élevées, de surveiller les volumes expirés et d’offrir une large gamme d’alarmes.
Les ventilateurs peuvent fournir une assistance respiratoire par le biais d’un circuit de fuite ou d’un circuit de valve.
Un circuit de fuite est un circuit unique qui comporte une fuite délibérée. Cette fuite peut se trouver dans le circuit lui-même ou dans le masque d’interface. Lorsque le patient expire, l’air expiré sort par la fuite. C’est pourquoi les appareils utilisés avec un circuit à fuite doivent toujours avoir un flux d’air passant par le circuit afin d’évacuer l’air expiré.
Une fuite non intentionnelle est une cause fréquente d’asynchronisme patient-ventilateur.
Les circuits à valve possèdent une valve d’inspiration et d’expiration active qui s’ouvre et se ferme avec l’inspiration et l’expiration. Les circuits à valve peuvent être utilisés pour la ventilation VI et VNI, en mode barométrique, volumétrique et mixte. Les circuits à valve peuvent être utilisés dans une configuration à un ou deux membres. Des masques non ventilés doivent être utilisés pour la ventilation non invasive par valve. Le circuit à deux membres peut être utilisé pour les patients dont le volume expiratoire doit être étroitement surveillé, comme les patients très jeunes ou ceux dont l’état est stable à un stade avancé. Les circuits à valve peuvent être utilisés chez les patients ventilés de manière invasive, mais ils peuvent également être utilisés de manière non invasive en mode barométrique et, dans certains cas, en mode volumétrique.
Recherche sur la ventilation non invasive à domicile
Explorez les enseignements principaux de la recherche clinique récente et comprenez leurs implications pour prendre des décisions thérapeutiques éclairées et sélectionner les patients appropriés.
Prise en charge des maladies respiratoires

Traiter la BPCO
Les directives internationales recommandent la VNI pour les patients BPCO hypercapniques stables, car elle peut améliorer la survie ainsi que la qualité de vie, et réduire le risque d’admission à l’hôpital.

Traiter le SOH
La VNI peut être recommandée pour les patients souffrant d’hypoventilation avec un SAOS léger ou nul, pour ceux qui souffrent d’hypertension pulmonaire comorbide et pour les personnes qui ne répondent pas au traitement CPAP.

Traiter les MND
La VNI nocturne peut améliorer les échanges gazeux, le sommeil, les symptômes et la survie des patients atteints de MND. La VNI diurne peut également s’avérer nécessaire pour les patients dont la maladie évolue.
Ce contenu est destiné uniquement aux professionnels de santé.
Veuillez vous référer aux guides d’utilisation et aux guides cliniques pour obtenir des informations pertinentes sur les contre-indications, les avertissements et les précautions à prendre avant et pendant l’utilisation des produits.
Références:
- M.L. Duiverman, J.M. Vonk, G. Bladder, J.P. van Melle, J. Nieuwenhuis, A. Hazenberg, et al.
Home initiation of chronic non-invasive ventilation in COPD patients with chronic hypercapnic respiratory failure: a randomised controlled trial. Thorax, 75 (2020), pp. 244-252 - R.J.M. van den Biggelaar, A. Hazenberg, N.A.M. Cobben, M.A. Gaytant, K.M. Vermeulen, P.J. Wijkstra.
“A randomized trial of initiation of chronic non-invasive mechanical ventilation at home vs in-hospital in patients with Neuromuscular Disease and thoracic cage disorder”: The Dutch Homerun Trial.Chest, (2020),
http://dx.doi.org/10.1016/j.chest.2020.07.007 - A. Hazenberg, H.A. Kerstjens, S.C. Prins, K.M. Vermeulen, P.J. Wijkstra.
Initiation of home mechanical ventilation at home: a randomised controlled trial of efficacy, feasibility and costs.
Respir Med., 108 (2014), pp. 1387-1395
http://dx.doi.org/10.1016/j.rmed.2014.07.008 | Medline - E. Bertella, P. Banfi, M. Paneroni, S. Grilli, L. Bianchi, E. Volpato, et al.
Early initiation of night-time NIV in an outpatient setting: a randomized non-inferiority study in ALS patients.
Eur J Phys Rehabil Med., 53 (2017), pp. 892-899
http://dx.doi.org/10.23736/S1973-9087.17.04511-7 - Duiverman ML. « Tricks and tips for home mechanical ventilation » Home mechanical ventilation: set-up and monitoring protocols. Pulmonology. 2021 Mar-Apr;27(2):144-150. doi: 10.1016/j.pulmoe.2020.08.002. Epub 2020 Sep 8. PMID: 32912752.
- Ahmed SM, Athar M. Mechanical ventilation in patients with chronic obstructive pulmonary disease and bronchial asthma. Indian J Anaesth. 2015 Sep;59(9):589-98. doi: 10.4103/0019-5049.165856. PMID: 26556918; PMCID: PMC4613406.
- Arnal JM, Thevenin CP, Couzinou B, Texereau J, Garnero A. Setting up home noninvasive ventilation. Chron Respir Dis. 2019 Jan-Dec;16:1479973119844090. doi: 10.1177/1479973119844090
- Contal O., Adler D., Borel J.-C., Espa F., Perrig S., Rodenstein D., Pépin J.-L., Janssens J.-P. Impact of different backup respiratory rates on the efficacy of noninvasive positive pressure ventilation in obesity hypoventilation syndrome: A randomized trial. Chest. 2013;143:37–46. doi: 10.1378/chest.11-2848.
- Cruz J, Brooks D, Marques A. Home telemonitoring effectiveness in COPD: a systematic review. Int J Clin Pract 2014; 68(3): 369-78.
- Arnal JM, Oranger M, Gonzalez-Bermejo J. Monitoring Systems in Home Ventilation. J Clin Med. 2023 Mar 10;12(6):2163. doi: 10.3390/jcm12062163.
- Jiang W, Jin X, Du C, Gu W, Gao X, Zhou C, Tu C, Chen H, Li H, Shen Y, Zhang Y, Ge X, Sun Y, Zhou L, Yu S, Zhao K, Cheng Q, Zhu X, Liao H, Bai C, Song Y. Internet of things-based management versus standard management of home noninvasive ventilation in COPD patients with hypercapnic chronic respiratory failure: a multicentre randomized controlled non-inferiority trial. EClinicalMedicine. 2024 Mar 10;70:102518. doi: 10.1016/j.eclinm.2024.102518.
- Wang T, Zhang L, Luo K, He J, Ma Y, Li Z, Zhao N, Xu Q, Li Y, Yu X. Noninvasive versus invasive mechanical ventilation for immunocompromised patients with acute respiratory failure: a systematic review and meta-analysis. BMC Pulm Med. 2016 Aug 27;16(1):129. doi: 10.1186/s12890-016-0289-y. PMID: 27567894; PMCID: PMC5002326.
Dernière mise à jour: 01.08.24